肺がんの病期(ステージ)と分類
肺がんの病期は
①最初に発生したがんの広がりや大きさの程度
②胸郭内や鎖骨の上あたりのリンパ節の状態
③離れた臓器への転移(遠隔転移)の有無
の3つの要素から決まります。病期は大きくI~Ⅳ期の4段階に分かれ、さらに同じ病期のなかで細かな分類があります(表1)。
小細胞肺がんの場合には、上記の病期に加え「限局型」と「進展型」の2つに分けることもあります。限局型とは肺の近くのリンパ節への転移があるものの、がんは片側の肺に留まっている状態のことを指します。進展型とは限局型の範囲を超えて広がっている状態のことをさします。
表1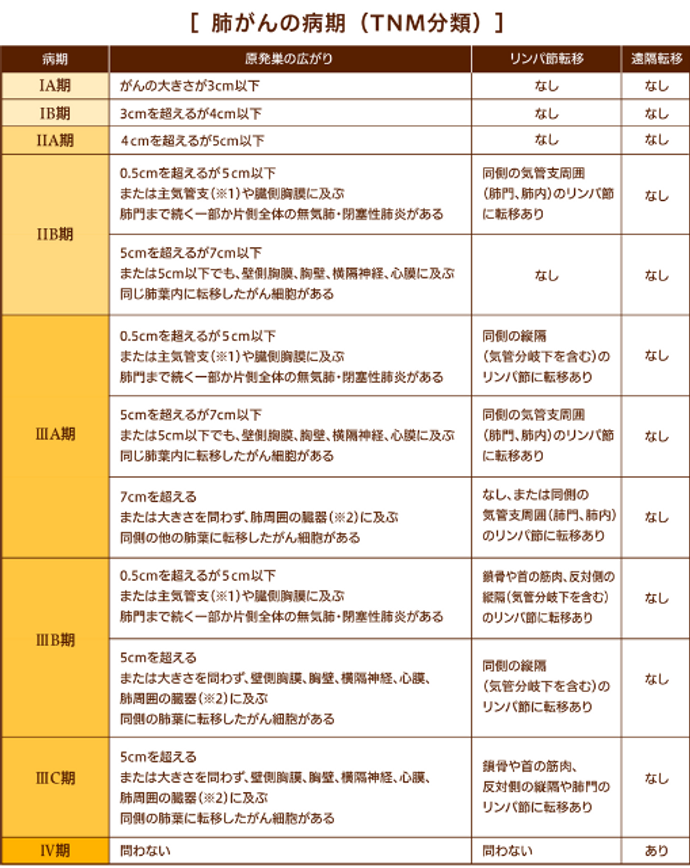 ⅠA期はさらにⅠA2期、ⅠA2期、ⅠA3期に、Ⅳ期はさらにⅣA期、ⅣB期に分類されます。
ⅠA期はさらにⅠA2期、ⅠA2期、ⅠA3期に、Ⅳ期はさらにⅣA期、ⅣB期に分類されます。
※1主気管支に及ぶが気管支分岐部には及ばない。
※2肺周囲の臓器:ここでは横隔膜、縦隔、心臓、大血管、気管、反回神経、食道、椎体、気管分岐部をさす。
※出典:日本肺癌学会 編. 肺癌取扱い規約 2017年1月 第8版. 金原出版, p3-11, 2017. より作成
肺がんの治療方針
医師は病期ごとの標準治療に基づいて治療法を検討します。とはいえ、がんの性質や病期が同じならばみんな同じ治療法というわけではありません。
身体状態(※注1)や年齢などによっても選択する治療法は変わります。もちろん患者さん自身がどのような治療を希望するかも大切です。納得して治療が受けられるよう担当医とよく相談しながら治療法を決めていきましょう。ここでは治療法について話し合う際に参考となる肺がんの標準治療について説明します。
※注1:身体状態を測る指標として、日常生活の活動度を「まったく問題なく活動できる」から「まったく動けない」までの5段階で評価する「パフォーマンスステータス」が使われています。その病期の標準治療であっても身体状態によっては体調悪化を早める可能性があるため治療ができるか見極めます。
非小細胞がん
比較的早期では、手術でがんのある肺葉の切除と周囲のリンパ節の切除(リンパ節郭清(かくせい)といいます)をするのが一般的です。手術が終わった後に、再発予防のため抗がん剤を使うこともあります。ある程度進行しているがんには、放射線治療か薬物療法を用います。状態がよい場合には放射線治療と薬物療法を併用することもあります。
<Ⅰ期>
基本的には手術を行います。手術の後に再発予防の目的で抗がん剤を使うこともあります。高齢の場合やからだの状態など何らかの理由で手術が難しい場合には、放射線治療を行います。
<Ⅱ期>
基本的には手術を行います。手術ができない場合には放射線治療、または放射線治療と抗がん剤治療を組み合わせた治療を行います。手術の後に再発予防の目的で抗がん剤を使うこともあります。
<Ⅲ期>
放射線治療と抗がん剤を組み合わせた治療が中心です。しかし、照射範囲が広く、根治照射が行えない場合には、抗がん剤治療単独になることもあります。なお、Ⅲ期の早い段階のがんでは手術を行うこともあります。
<Ⅳ期>
細胞障害性抗がん剤のほか、遺伝子検査の結果によって分子標的や免疫チェックポイント阻害剤を使うこともあります。
小細胞肺がん
限局型は放射線治療と薬物療法を組み合わせた治療が中心ですが、ごく早期には手術を行うこともあります。進展型には薬物療法や緩和ケアが標準治療となります。
肺がんの手術とは
肺がんの手術の標準的な治療はがんのある肺葉を切除する方法です。実際にどのくらいの範囲まで肺を切除するかは、がんの状態と身体的負担とのバランスで決めます。肺の手術には切除する範囲によって次の3つに分けられます。
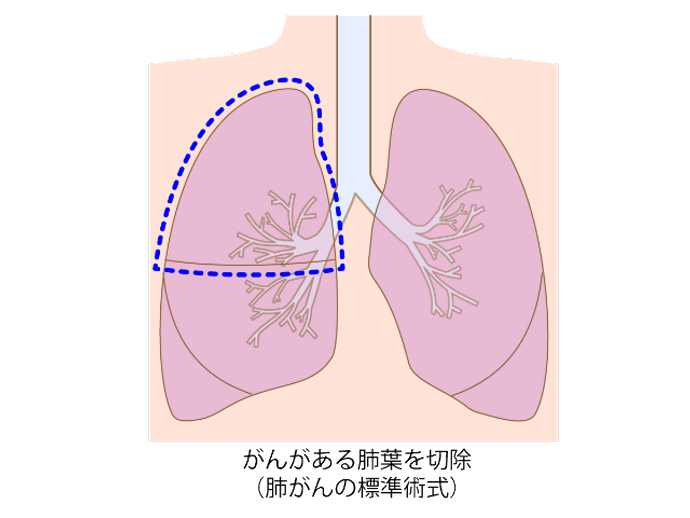
肺葉切除術
がんのある肺葉を切除する方法です。通常はがんが移転している可能性のある肺の周囲のリンパ節も切除(リンパ節郭清)します。I期・Ⅱ期の非小細胞がんに対する標準的な治療法です。
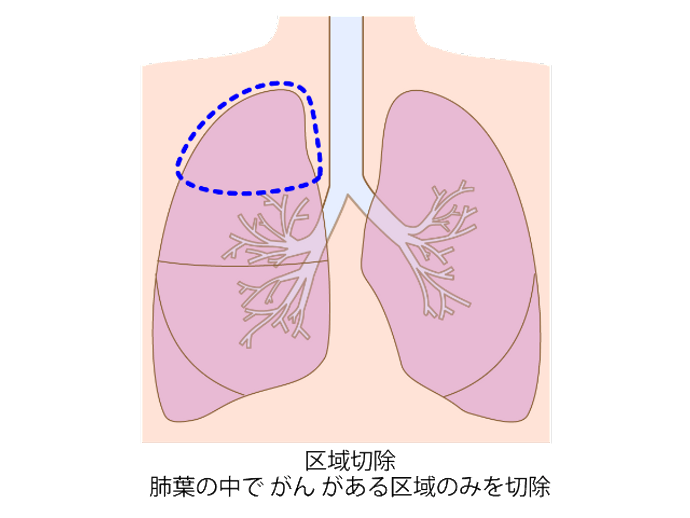
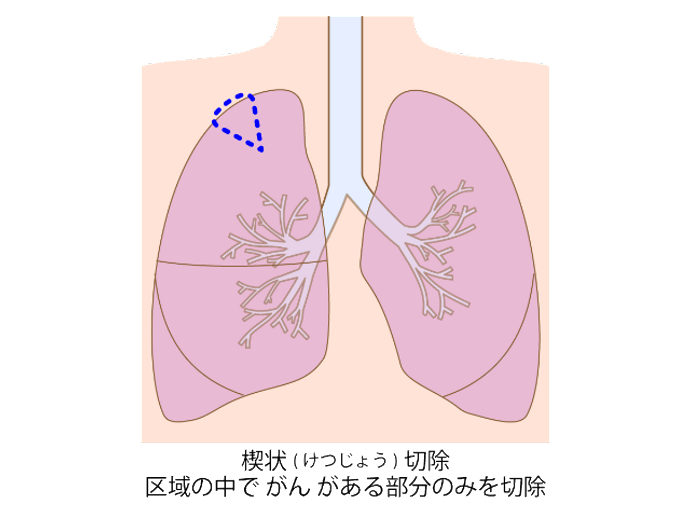
縮小手術
肺をできる限り温存するため、がんが発生している肺葉の一部を切除する方法です。縮小手術には、がんの周辺を切除する「区域切除」と、それよりさらに切除する範囲をがんの部分だけに狭めた「楔状(けつじょう)切除」があります。
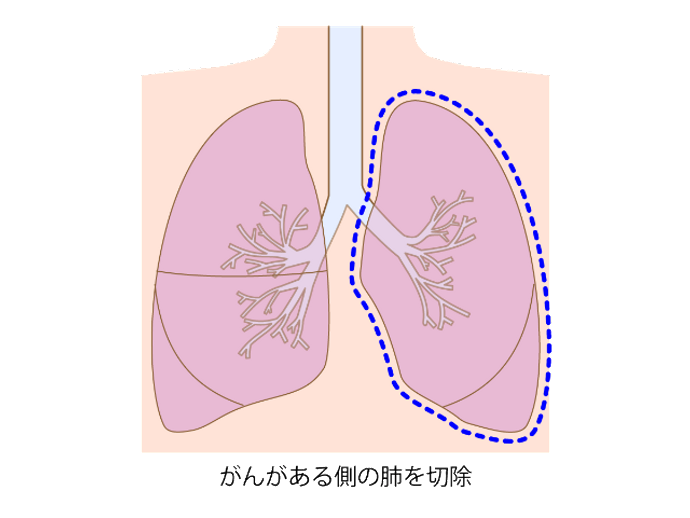
片肺全摘手術
片側の肺を全て切除する方法です。がんが肺葉を超えて広がり気管支などに及んでいる場合に行います。からだへの負担が大きいため心臓や肺の状態、年齢などを考慮して手術するかどうか判断します。
・がんを目視する「開胸手術」とカメラを使う「胸腔鏡手術」
従来は15cm以上切開する開胸手術が主流でしたが、最近は胸腔鏡というビデオカメラを肋骨の間から挿入し、画面で内部を確認しながら肺を切除する方法での手術が増えています。また、2018年に保険適用されたロボットを用いた胸腔鏡手術も普及しつつあります。ただし、胸腔鏡手術の方が優れているというわけでもありません。胸腔鏡手術は傷跡が小さくて済みますが、開胸手術と比べると血管を傷つけた時の対応が遅れるリスクもあります。それぞれの方法に利点と欠点がありますので、手術法を選択する際は担当医とよく話し合って決めましょう。
・手術後は1週間程度で退院できることが多い
手術後、切除した肺の部分には血液や空気がたまるためドレーンと呼ばれる管を入れて吸引します。手術後2~4日経てばドレーンを外せます。医療機関によって異なりますが、手術から約1週間程度で退院することができます。ひとつの肺葉を切除した場合、肺活動は2~3割落ちますが1年ほど経つと手術前と同程度まで回復することもあります。
肺がんの放射線治療とは
放射線治療をすると決まったら、まず放射線腫瘍医治療計画を立てます。治療に用いる高エネルギーのX線は、がんに照射できれば確実な効果が得られますが、周辺の正常細胞にダメージを与える可能性もあります。そこで予め照射範囲や方向を決めておくのです。照射量や回数は、放射線治療の目的によっても変わります。
一般的に非小細胞がんの治療では、1回あたり決められた放射線量の照射を週5回、合計6週間行います。一方、小細胞がんの場合には1日の照射回数を増やし、照射期間を短くすることで治療効果が高まることが知られています。
・がんの状態や広がりの程度に応じて照射方法を選択
放射線機器の進歩で、がんに高線量を集中的に照射する技術も以前より高くなっています。がんに対して多方向から狙い撃ちする「定位放射線治療(ピンポイント照射)」は安全に高線量照射ができ、早期の肺がんの場合、従来の放射線治療と比べ良好な治療成績が得られることがわかっています。
そのほかのがん全般に用いられるのはがんの形や位置に合わせて放射線を照射する「三次元原体照射」で、リンパ節などへの照射が必要になる病状の進んだ非小細胞がんなどにも用いられます。さらに最近は、三次元原体照射よりも複雑な形の線量分布の調整ができる「強度変調放射線治療(IMRT)」ができる施設も増えてきています。どの照射方法を選択するかは、がんの状態や広がり、からだの状態などを踏まえて決めてゆきます。
・治療が終わってからも定期的に検診を受けましょう
放射線治療は手術などと比べると負担は少ないものの、治療途中や治療後に副作用が生じることがあります。治療中から治療終了直後に見られる副作用としては、皮膚炎、食道の痛みや飲み込みにくさ(放射線性食道炎)、咳や発熱(放射線性肺炎)などがあります。これらの副作用は治療数カ月後から数年後に表れることもあるため、治療が終わった後も定期的な検診が必要です。
肺がんの薬物治療とは
がんの遺伝子タイプ別の分子標的薬を筆頭に、肺がんの薬物療法の進化は日進月歩です。飲み薬での治療や副作用対策が進み、治療を続けながらもその人らしい生活を送れるようになってきました。2019年には薬物療法の治療選択に必須である遺伝子検査が保険適用になっています。肺がんが進行していても治療選択肢があり、より一人ひとりに合ったいわば“テーラーメイド型”の治療を受けられる仕組みづくりが進んでいます。
・非小細胞がんと小細胞がんの薬物療法の流れ
治療にどのような薬を使うかは肺がんの種類や病期、からだの状態などによって変わります。ここでは非小細胞がんと小細胞がんのそれぞれ標準的な治療の流れを説明します。
・非小細胞がんの薬物療法
一般的に抗がん剤などを投与する場合には、何日間か投与した後一定の期間休養(休薬)をとって再び投与するという形で治療が進められます。非小細胞がんの場合、よくみられるのは3~4週間を1サイクルとし、それを4~6サイクル繰り返す方法です。
抗がん剤、分子標的薬、免疫チェックポイント阻害剤といった治療薬から何を選択するかは、遺伝子検査やPD-L1検査の結果を踏まえて決めます。治療を続けるなかで薬の効果が薄れた場合には、次に有効性が高いと考えられる別の薬を使って治療を行います。
・小細胞がんの薬物療法
小細胞がんは進行が早い反面、抗がん剤が効きやすいという特長があります。手術でがんを取り切れる限局型の場合は再発・転移予防のために手術後に抗がん剤を使用します。限局型でも手術ができない場合は抗がん剤を複数組み合わせる併用療法と放射線治療を並行して行います。
進展型の場合は、抗がん剤の併用療法のみでの治療が標準治療です。抗がん剤を中心に行われていますが、最近、免疫チェックポイント阻害剤の使用も保険適用になりました。さらに現在、新しいタイプの抗体薬(※1)の開発や小細胞がんの発生や増殖に直接関わる遺伝子を検出する研究も進んでいます。
※1:抗体薬とは、病気の原因となる物質に対する抗体を人工的につくり体内に入れることで予防・治療を行う薬のことです。
薬物治療の薬の働き
肺がんの薬物治療に用いる3つの薬剤が、それぞれどのような働きをするのか見ていきましょう。
細胞障害性抗がん薬(抗がん剤)
がん細胞の増殖の仕組みの一部に作用しがん細胞を攻撃する薬です。抗がん剤はがん細胞だけでなく正常な細胞に対しても作用するため副作用があります。
抗がん剤の投与量が増えればからだへの負担も大きくなるため、抗がん剤の投与量やスケジュールは効果と副作用のバランスが最適になるよう慎重に評価します。抗がん剤は一般的に点滴での投与で、初回の抗がん剤治療は入院が必要なことが多いですが、最近は通院での治療もできるようになってきています。
分子標的薬
がん化やがんの増殖の原因となる「ドライバー遺伝子」を目印として、がん細胞を攻撃する治療薬です。ドライバー遺伝子とは、がんの発生や進行に直接関わる「運転手」の役割をする遺伝子で、この遺伝子に異常があると本来働くはずのがん化を抑えるブレーキが利かずがん細胞が増殖し続けます。
そのメカニズムに着目した薬が分子標的薬です。肺がんのドライバー遺伝子の異常でもっとも多いのは「EGFR遺伝子」の変異で、肺がん全体の約3割に見られます。そのほかにも「ALK融合遺伝子」、「ROS1融合遺伝子」「BRAF遺伝子」「MET遺伝子」「NTRK融合遺伝子」「RET融合遺伝子」などの遺伝子異常が知られています。
分子標的薬の治療を行う際には必ず遺伝子検査を行い、それぞれに合った分子標的薬で治療します。一般的に分子標的薬は抗がん剤と比べて副作用の影響が小さく、高い治療効果が見られ、また、治療が困難な副作用が生じない限り、継続して治療を続けます。なお、分子標的薬の適応は、今のところ非小細胞がんに限られています。
免疫チェックポイント阻害剤
私たちには、ウイルスや細菌など異物に攻撃してからだを守る免疫機能が備わっています。一方で、免疫機能が過剰に働いて自分のからだを攻撃しすぎないように免疫チェックポイントで攻撃するかどうか判断して、異物に対する攻撃にブレーキをかける仕組みもあります。
がん細胞はその免疫の仕組みを巧みに利用し免疫細胞からの攻撃をかわしています。このようながん細胞の性質に着目したのが、免疫チェックポイント阻害剤です。
免疫チェックポイントにはいくつか種類がありますが、そのひとつである免疫チェックポイント受容体PD-1にがん細胞にあるPD-L1がくっつくと、免疫機能にブレーキがかかります。そのPD-1にがん細胞より先に結合し免疫にブレーキがかかるのを阻止し、がんを攻撃する力を回復させるのが免疫チェックポイント阻害剤です。免疫チェックポイント阻害剤の治療をする前には、肺がん細胞の表面にPD-L1がどの程度あるか検査した上で、治療法を選択します。
薬物治療(抗がん剤)の副作用とは
抗がん剤の治療をすると、数日以内に吐き気や嘔吐、食欲不振などの症状が現れることがあります。1週間ほどすると、骨髄抑制といって血液を作る働きが衰えたり肝機能や腎機能が低下したりすることもあります。数週間後には髪の毛が抜け、手足のしびれや耳鳴りなどの神経症状が出ることもあります。こうした副作用の症状は個人差もあり、使用する薬剤によっても変わってきます。
緩和ケアによる副作用の予防や吐き気を抑える制吐剤が使えるようになってはいますが、副作用に対して不安や心配な気持ちを持つのは当たり前のことです。治療をはじめる際には、いつどんな副作用が起こりやすいのか、そのための対策はあるか、とくに注意すべき症状はどんなものか、またどんな不安を持っているのかなど担当医に相談しましょう。
さまざまな副作用への対処について、詳しくは「各症状への対処」https://www中カテゴリトップURLを参照してください。
【参考文献】
国立がん研究センターウェブサイト 肺がん
https://ganjoho.jp/public/cancer/lung/index.html
「国立がん研究センターの肺がんの本」(小学館クリエイティブ)
「患者さんのための肺がんガイドブック 2019年版」(金原出版)


